下面我们就一起来借鉴一下这篇纯测序的m6A修饰谱文章的分析思路。

发表日期:2021年9月17日
影响因子:7.691
研究方法:LC-MS/MS、m6A MeRIP-seq、RNA-seq、MeRIP-qPCR (均由云序生物提供)
文章链接:Transcriptome-wide Dynamics of m6A mRNA Methylation During Porcine Spermatogenesis
技术路线

为了获得精子发生过程中m6A的转录组宽图谱,首先使用STA-PUT速度沉淀法从猪睾丸中分离出精原细胞SPG、精母细胞PS和圆形精子RS,并用免疫细胞化学分析验证了新鲜分离的生殖细胞是具有生化和核特征的SPG、PS和RS。为了阐明精子发生不同阶段的m6A甲基组,进行了液相色谱-串联质谱LC-MS/MS(云序提供此服务)以量化分离的生殖细胞中整体m6A修饰的变化,m6A水平在发育阶段保持相对稳定(~0.3%)。
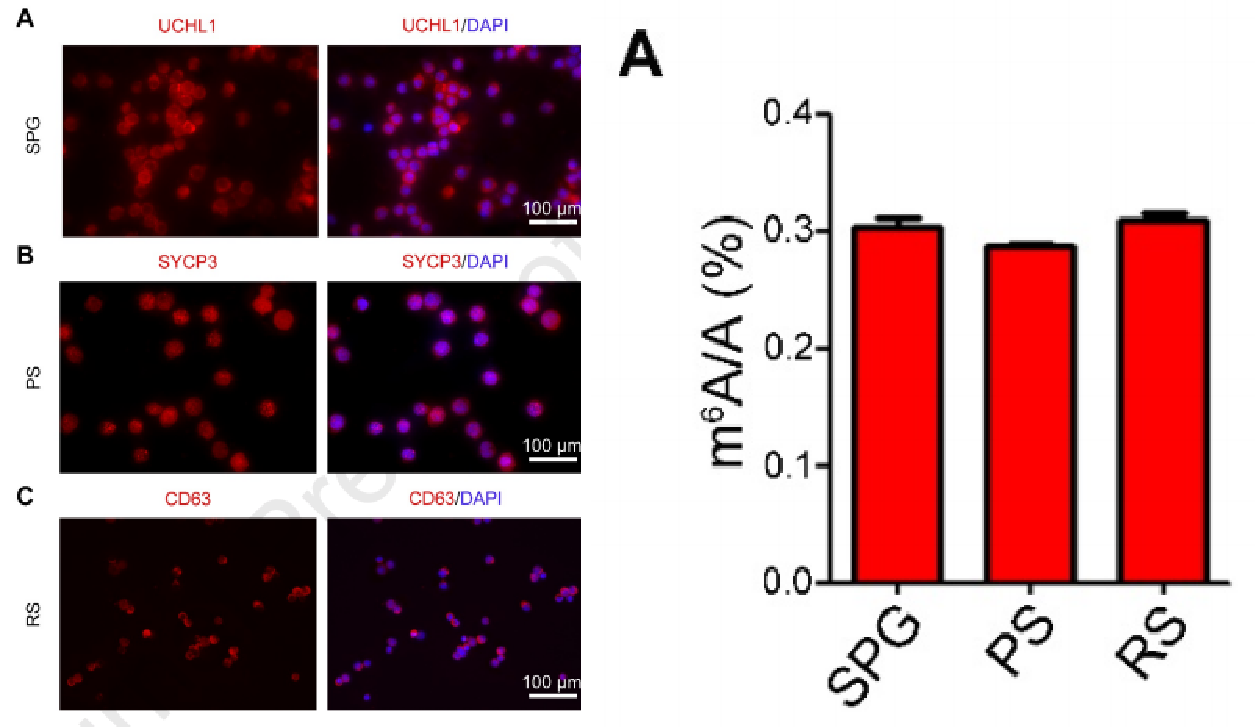
二、猪雄性生殖细胞m6A修饰谱
为了进一步揭示m6A的动力学,进行了m6A MeRIP-seq(云序提供此服务)。分析结果显示,m6A峰在生殖细胞的起始密码子(startC)、编码序列(CDS)和终止密码子(stopC)附近高度富集,m6A读数分布在整个mRNA转录本中,其中读数在CDS中增加,并在3'UTR处达到峰值。但是m6A峰分布在生殖细胞的三个阶段之间存在一些差异,SPG的3'UTR中的m6A读数密度高于PS和RS中的m6A读数密度。总之,结果表明,m6A在猪雄性生殖细胞中是动态的,这表明它在精子发生过程中起着关键作用。另外为了确定RRACH是否是猪生殖细胞中的m6A共有序列,作者分析了1000个最显著的峰。GGACU是所有测试样本中的顶级基序,表明猪精子发生中采用的RRACH基序在猪和小鼠中是保守的。值得注意的是,作为SPG、PS和RS中的顶部基序,GGACU是一种普遍存在于猪雄性生殖细胞中的m6A修饰序列
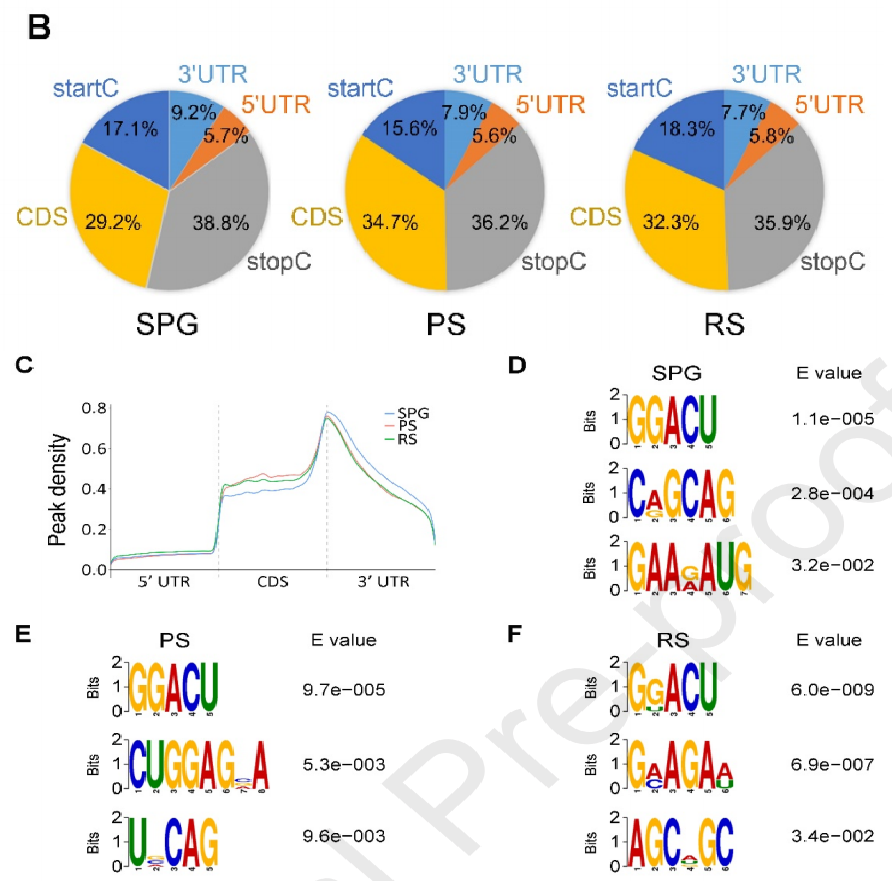
三、富含m6A的基因参与重要的生物过程
作者在猪雄性生殖细胞中共发现了11241个甲基化基因。其中,2378、277和841个甲基化基因分别在SPG、PS和RS中特异表达。基因本体生物学过程(GO)分析显示4886个持续甲基化的基因主要参与代谢过程。然后,作者又分析了m6A修饰水平差异的基因,结果表明,4354个基因是SPG和PS之间的差异甲基化基因(DMG),在PS和RS的比较中,也有3058个RS中高甲基化基因和884个低甲基化基因。GO分析显示,PS中的甲基化上调基因(与SPG相比)参与精子发生,而甲基化下调基因主要参与代谢过程。此外,RS(与PS相比)中的高甲基化基因参与发育和代谢过程,而低甲基化基因主要参与染色体组织、核酸代谢和微管基础过程的调节。
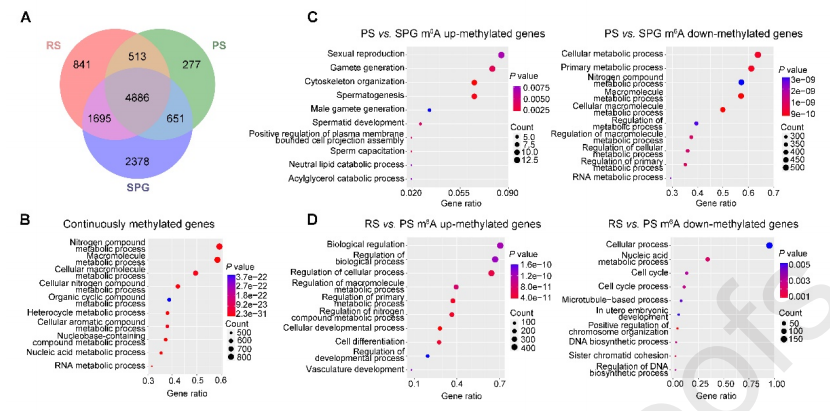
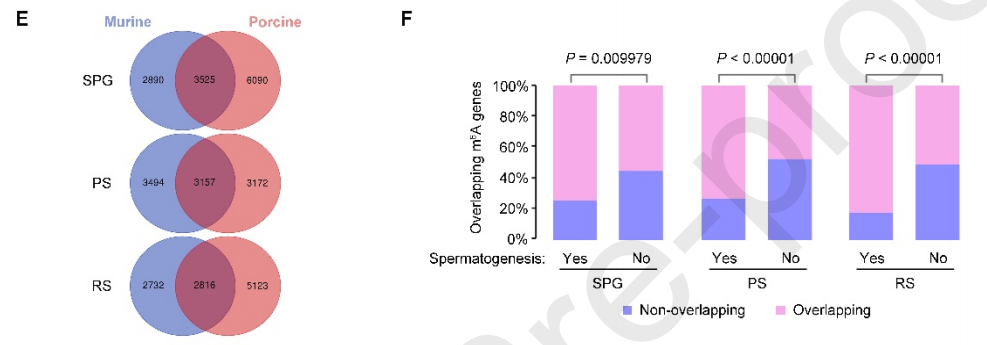
除此之外,作者对来自猪和小鼠生殖细胞的m6A修饰基因进行了比较。分别在猪SPG、PS和RS中发现总共6090、3172和5123个m6A修饰基因,而小鼠和猪SPG、PS和RS分别共享3525、3157和2816个m6A修饰基因。值得注意的是,这些重叠的m6A甲基化转录物优先富集,并被报告为对小鼠精子发生至关重要,表明m6A介导雄性生殖细胞中的保守过程。
四、精子发生过程中的基因表达
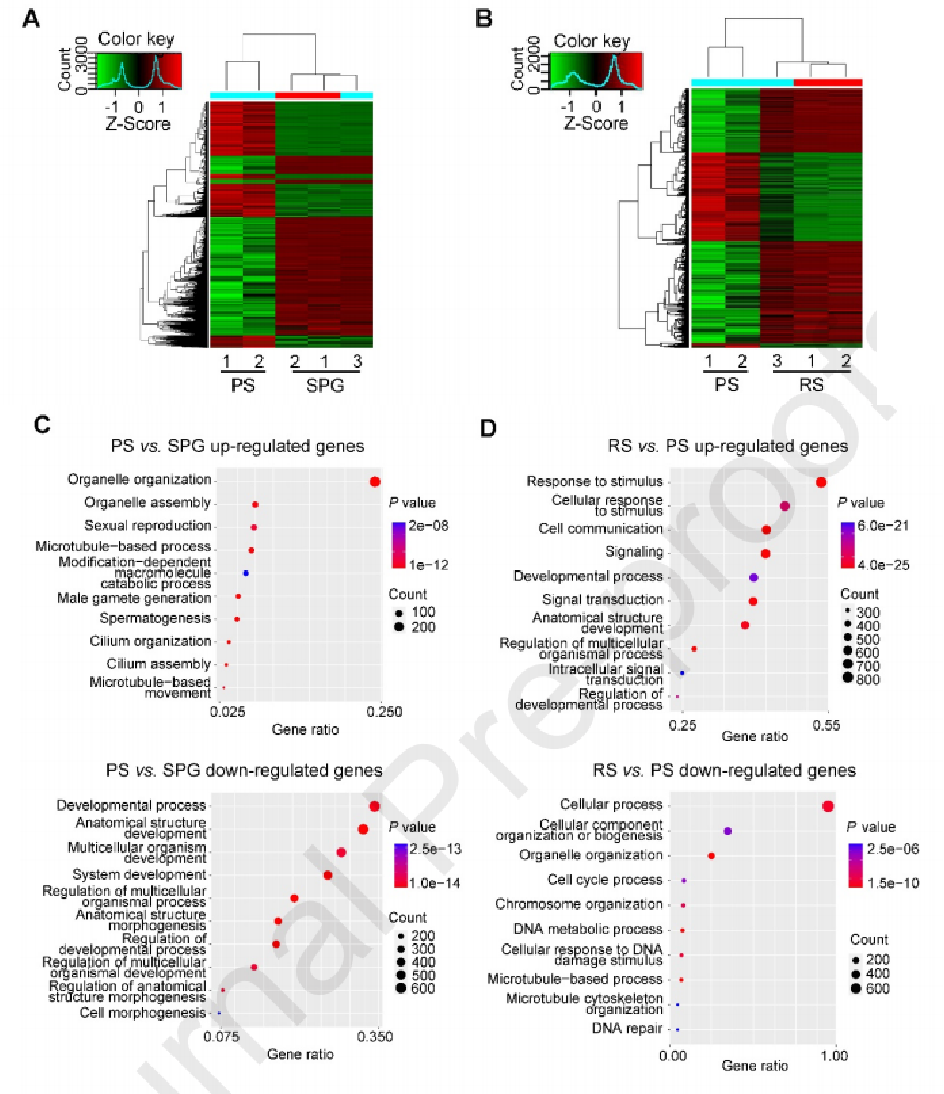
为了进一步探索m6A的调节作用,作者对这些生殖细胞进行了RNA-seq(云序提供此服务),分析了在持续发育的生殖细胞之间差异表达的基因(DEG)。在SPG和PS之间共鉴定出10342个DEG,其中4393个上调,5949个下调。在RS和PS中,5119个上调基因和2872个下调基因差异表达。GO富集分析显示,在PS中,上调基因(与SPG相比)主要参与纤毛组织和精子发生,而下调基因则参与解剖结构形态发生和发育过程的调节。在RS中,上调基因主要调控细胞通讯和发育过程,而下调基因则调控染色体组织和DNA代谢过程。结合m6A修饰差异基因的功能,作者提出m6A修饰可能影响基因表达,从而调节精子发生。
五、m6A修饰参与调节基因表达
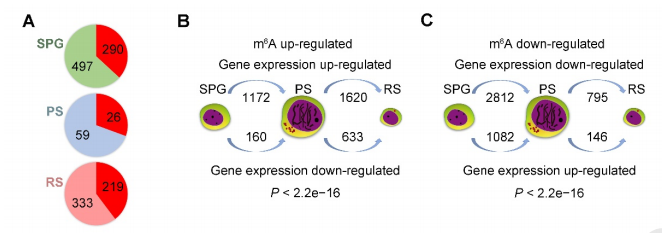
作者发现36.8%、30.6%和39.7%的阶段特异性转录本带有m6A修饰。为了探讨m6A修饰是否会影响基因表达,作者对每个相邻阶段之间的DMGs和DEGs进行了联合分析,发现m6A修饰水平与基因表达倾向于正相关。
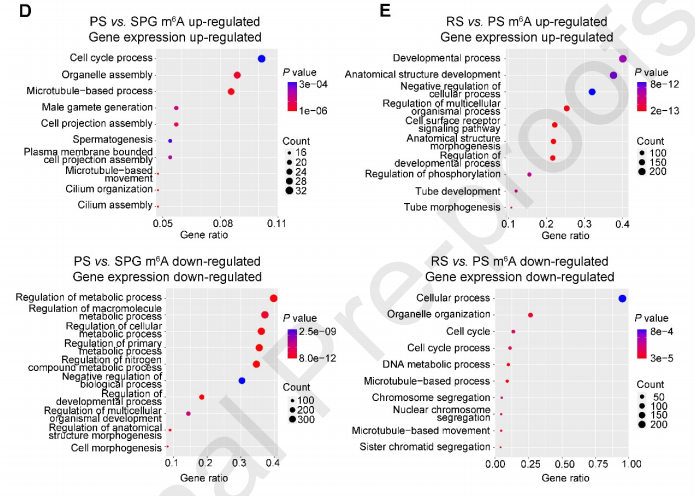
为了进一步揭示动态修饰的m6A基因的生物学意义,作者对修饰水平和表达水平呈正相关的基因进行了GO分析,发现在PS中,上调基因主要参与精子发生和微管基础过程的调节,而下调基因则参与代谢过程和发育过程的调节。在RS中,上调基因调控发育过程和管形态发生,下调基因参与姐妹染色单体分离、DNA代谢过程和微管基础过程。这些发现表明m6A介导基因表达并调节精子发生。
六、m6A介导的基因表达与SSC的命运相关
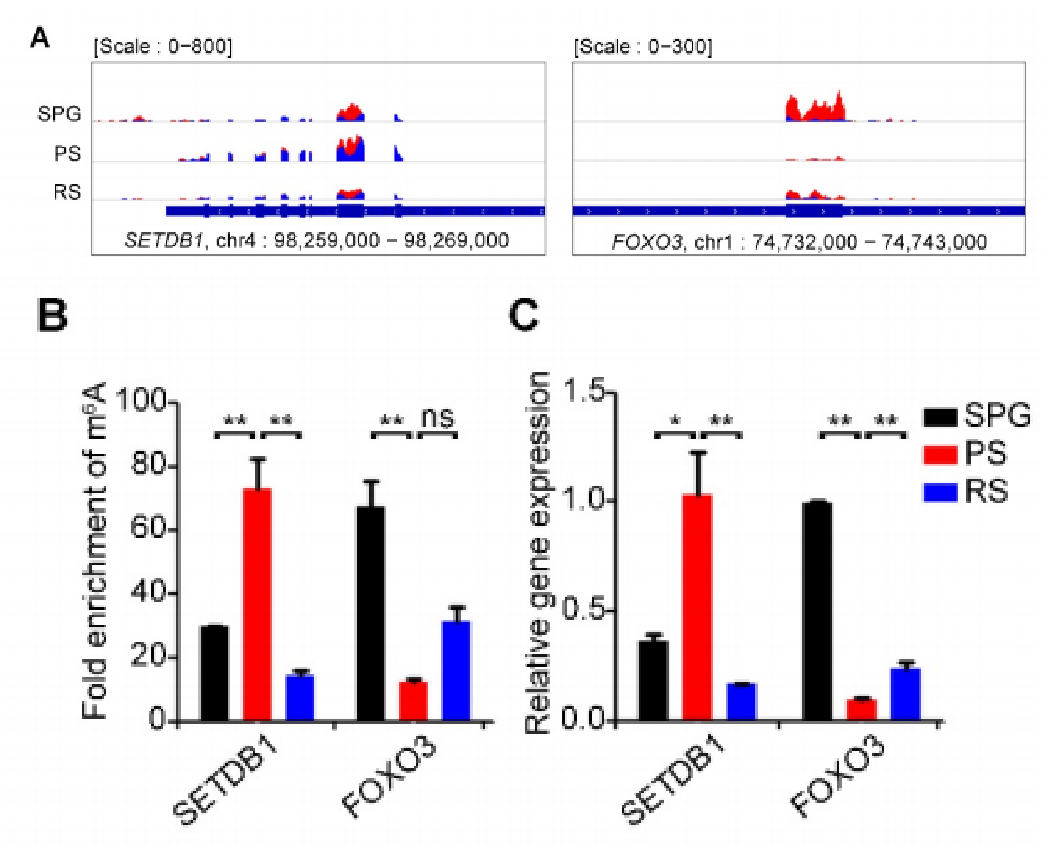
先前的研究表明,甲基转移酶集合结构域分叉的组蛋白赖氨酸甲基转移酶1(SETDB1)催化组蛋白H3赖氨酸9(H3K9me3)的三甲基化,并对精原干细胞(SSC)存活起重要作用。同时,FOXO1、FOXO3和FOXO4的缺陷会损害SSC的自我更新和分化。为了确定m6A是否介导这些基因的表达,作者首先从m6A MeRIP-seq(云序提供此服务)数据中观察到SETDB1和FOXO3转录本至少包含一个m6A峰。然后通过MeRIP-qPCR(云序提供此服务)验证到在SPG到PS到RS这个发育过程中,SETDB1基因的m6A修饰先上调再下调,而FOXO3基因的m6A修饰先下调再上调。qPCR验证结果显示两个基因的表达水平与m6A修饰水平的改变呈强正相关。
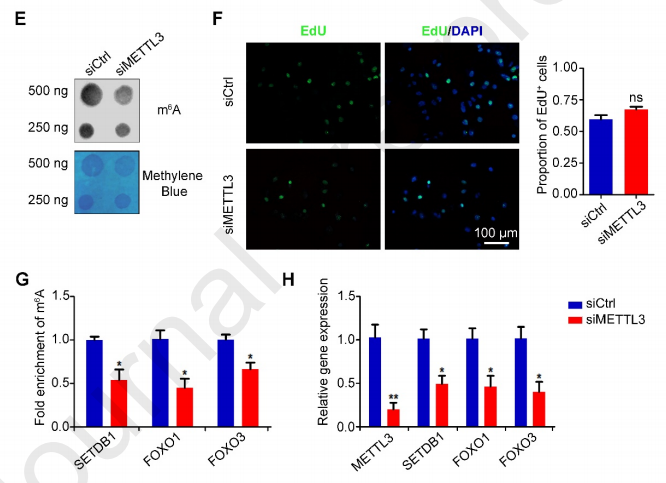
为了进一步验证m6A的调节作用,作者通过小干扰RNA(siRNA)在猪SSC中敲除甲基化酶METTL3。与对照组(siCtrl)相比,METTL3的敲除(siMETTL3)导致整体m6A水平降低,不过显示siCtrl和siMETTL3之间的细胞增殖未发现显著差异。MeRIP-qPCR(云序提供此服务)显示,METTL3基因敲除显著降低了SETDB1、FOXO1和FOXO3中m6A水平。此外,qPCR分析显示这三个靶基因表达显著下调,与RNA-seq(云序提供此服务)数据显示的SPG和PS动态一致。因此,这些数据表明m6A在猪精子发生过程中介导动态基因表达。
这篇文章首次展示了猪精子形成过程中的m6A修饰图谱。对分离出的猪精原细胞(SPG)、精母细胞(PS)和圆形精子(RS)进行LC-MS/MS m6A整体水平检测,m6A MeRIP-seq和RNA-seq,通过分析m6A的丰度和基因表达,结合甲基化酶敲降和MeRIP-qPCR验证,首次阐明了m6A在猪精子发生过程中的转录调控作用,为今后将m6A与男性不育的研究和治疗打下基础。
对m6A RNA甲基化,目前最流行的检测手段为m6A-Seq技术,适用于m6A RNA甲基化谱研究,快速筛选m6A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m6A测序:
- m6A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- m6A LncRNA测序(涵盖LncRNA和mRNA)
- m6A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- m6A mRNA测序
- m6A miRNA测序
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法检测整体RNA修饰水平
快速检测m6A整体甲基化水平
03 m6A RNA修饰上游酶的筛选
m6A RNA修饰相关酶PCR芯片
寻找上游直接调控m6A RNA甲基化的甲基转移酶。
04 m6A RNA修饰靶基因验证
MeRIP-qPCR
云序提供各类不同修饰的MeRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。
05机制互作研究
5.1 RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
5.4ChIP-seq
筛选或验证目标蛋白与DNA互作,研究相应的分子调控机制。
优势一:发表10分以上文章最多的m6A RNA甲基化测序服务平台。云序已累计支持客户发表56+篇高水平RNA修饰文章,合计影响因子480分+,是国内支持发文最多、累计影响因子最高的公司。
优势二:至今完成4000+例 m6A测序样本,全面覆盖医口、农口等各类样本。
优势三:全面检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:独家提供m6A一站式服务:m6A整体水平检测、m6A测序、MeRIP-qPCR验证、RIP和RNA pull-down等。等。
优势五:率先研发超微量MeRIP测序技术,RNA量低至500ng起。
优势六:国内最全的RNA修饰测序平台,提供m6A、m5C、m1A、m7G、m3C、m6Am、O8G、ac4C乙酰化和2'-O-甲基化测序。
相关产品
往期回顾
项目文章|赫捷院士团队揭密肺腺癌 m6A 机制再次登上Nature 子刊!
上海云序生物科技有限公司 商家主页
地 址: 上海市松江区莘砖公路518号24号楼4楼
联系人: 戴小姐
电 话: 021-64878766
传 真: 021-64878766
Email:market@cloud-seq.com.cn;liuqingqing@cloud-seq.com.cn
相关咨询
杨宝峰院士团队RNA修饰又一成果 | 云序ac4C acRIP-seq助力揭示心脏I/R损伤的作用机制 (2024-12-03T00:00 浏览数:11217)
杨宝峰院士团队最新成果 | 云序助力揭示RNA修饰m7G调控心肌肥厚的机制研究 (2024-11-13T00:00 浏览数:12786)
Nature子刊| 重磅综述!一文总结「m6A修饰非编码RNAs」在各类肿瘤中的调控机制及作用 (暂无发布时间 浏览数:10716)
研究速览-eccDNA 2023年最新进展大放送! (暂无发布时间 浏览数:11381)
云序生物MeRIP-qPCR技术干货 (暂无发布时间 浏览数:11273)
技术干货| “eccDNA碱基序列的获取及引物设计”方法教程 (暂无发布时间 浏览数:10658)
云序客户m6A高分文章|揭示组蛋白乙酰化与m6A修饰在眼部黑色素瘤发生中的共同作用机制 (暂无发布时间 浏览数:5987)
Nat Biotechnol IF=47 | BID-seq:一种基于单碱基分辨率的假尿嘧啶(Ψ)修饰定量测序检测方法 (暂无发布时间 浏览数:5848)
北大伊成器团队Nature Reviews重磅发文:非m6A热门修饰调控与功能一文速览! (暂无发布时间 浏览数:9025)
用户文章m6A专题|IF=9.8|m6A去甲基化酶ALKBH5缺乏会加重钴致神经退行性损伤 (暂无发布时间 浏览数:5854)
